Nuevo enfoque permite a los científicos encontrar indicios de la existencia de células madre cancerosas
> Artículo en inglés
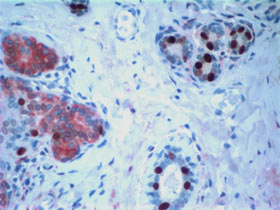 Tejido de cáncer de mama con una mutación del gen BRCA1. Las células madre aparecen en rojo y el receptor de estrógeno en marrón. Un racimo de células madre ampliadas en la izquierda muestra la expresión reducida del receptor de estrógeno en comparación con los lobulillos normales en la derecha. (Cortesía del Centro Oncológico Integral de la Universidad de Michigan).
Tejido de cáncer de mama con una mutación del gen BRCA1. Las células madre aparecen en rojo y el receptor de estrógeno en marrón. Un racimo de células madre ampliadas en la izquierda muestra la expresión reducida del receptor de estrógeno en comparación con los lobulillos normales en la derecha. (Cortesía del Centro Oncológico Integral de la Universidad de Michigan).Con la ayuda de herramientas genéticas, investigadores han identificado subconjuntos de células que parecen impulsar el crecimiento de tumores en ratones. Los hallazgos, provenientes de tres estudios independientes, ofrecen factores adicionales que sustentan la hipótesis de la existencia de células madre del cáncer, es decir, la idea de que algunos tumores contienen células que se autorenuevan y dan origen a todo tipo de células tumorales. Dos de los estudios aparecieron el 1 de agosto en Nature mientras que el tercero fue publicado el mismo día en Science.
Cada grupo de investigadores utilizó las herramientas genéticas para "etiquetar" las células tumorales y rastrear su ascendencia en un ratón modelo diferente. Los resultados de cada uno de los estudios parecen indicar que al menos algunos tumores contienen ciertas poblaciones de células que impulsan el crecimiento y la supervivencia del tumor. Éstas serían las células madre cancerosas, también conocidas como células iniciadoras del tumor.
"Los tres estudios ofrecen nuevos e interesantes elementos que sustentan la hipótesis de la existencia de las células madre cancerosas", dijo el doctor Max Wicha, director del Centro Oncológico Integral de la Universidad de Michigan e investigador de las células madre cancerosas, quien no participó en ninguno de los tres estudios. "Se trata de estudios que plantean retos técnicos y están muy bien hechos".
Resistencia a la quimioterapia
Los autores de uno de los informes publicados en Nature identificaron una población de células de tumores cerebrales que permitían que los tumores cerebrales reaparecieran después del tratamiento con el fármaco temozolomida. Al principio, el fármaco agotó la proliferación de las células cancerosas, lo cual desaceleró el crecimiento tumoral, pero no afectó una población de células menos activas, es decir, las células madre cancerosas. Como consecuencia de ello, los tumores reaparecieron.
"Nosotros creemos que ésta es una demostración clara y rigurosa de que la hipótesis de la existencia de las células madre cancerosas está viva y es válida en al menos un tumor sólido", dijo el investigador principal, doctor Luis F. Parada del Centro Médico Southwestern de la Universidad de Texas en Dallas. "El tiempo dirá con qué frecuencia este mecanismo tumoral podrá explicar la existencia de otros tumores sólidos".
El segundo estudio publicado en Nature identificó poblaciones distintas de células cancerosas en un ratón modelo utilizado para investigar la aparición de los tumores de la piel. En concordancia con la hipótesis de la existencia de células madre cancerosas, una población relativamente pequeña de células de tumores duraderos dio finalmente origen, durante el crecimiento del tumor, a células hijas, las cuales formaban una parte substancial del tumor.
"El nuevo método de rastrear el destino de las células tumorales in situ ha demostrado la existencia de células madre cancerosas que alimentan el crecimiento de los tumores in vivo", dijo en un correo electrónico el investigador principal, doctor Cedric Blanpain de la Universidad Libre de Bruselas.
El tercer estudio, publicado en Science, encontró indicios de células madre cancerosas en lesiones intestinales precancerosas en ratones. Aun cuando los tres estudios apuntan a la existencia de células madre cancerosas, aún no se conocen las implicaciones de los hallazgos en ratones en los tumores en seres humanos.
Avances en este campo
Descubiertas por primera vez en la leucemia, se han reportado células madre cancerosas en tumores sólidos tales como cáncer de cerebro, mama y colon. Los indicios de la existencia de estas células provienen en primer lugar de experimentos en los cuales solamente una pequeña proporción de células tumorales humanas pudieron proliferar extensamente y formar nuevos tumores cuando las células fueron trasplantadas a ratones.
Pero hay otros factores, además de las células madre cancerosas, que podrían explicar la formación de nuevos tumores a partir del trasplante de ciertas células, argumentaron los investigadores. La formación o no de tumores en ratones podría depender de la manera como se hizo el trasplante y el tipo de ratón modelo utilizado en el experimento.
Hay que tomar en cuenta demasiadas variables para poder sacar conclusiones definitivas acerca de las células madre cancerosas a partir de estos experimentos con trasplantes, señaló el doctor Parada. El surgimiento de herramientas genéticas para codificar las células tumorales ofreció la oportunidad de estudiar posibles células madre en sus ambientes naturales.
"En los nuevos estudios se abandona la idea de que se ven las células madre cancerosas solamente si uno altera el tumor humano y se lo trasplanta a un animal", dijo el doctor Wicha. "Estos dos nuevos hallazgos permitirán avances en este campo".
Los resultados también parecen indicar que las mismas vías utilizadas en la generación de tejidos normales podrían ser activas en la formación de tumores. "La jerarquía celular encontrada en la evolución inicial del tumor es una corrupción de la jerarquía celular encontrada en tejidos normales", afirmó el doctor Blanpain.
Implicaciones clínicas
El concepto de la existencia de células madre cancerosas tiene posibles implicaciones en los tratamientos. Si estas células existen en los tumores humanos, tendrían que ser erradicadas a fin de lograr la supervivencia a largo plazo. A juzgar por los nuevos estudios, para "curar un cáncer es necesario poder identificar las células madre cancerosas y actuar sobre ellas", dijo el doctor Parada.
Ya hay varias docenas de estudios clínicos que están analizando los métodos para actuar sobre las células con propiedades similares a las de las células madre en los pacientes, según el doctor Wicha. Sin embargo, incluso con los nuevos hallazgos, es probable que persista la controversia en relación con las células madre cancerosas. Sin embargo, como dijo el doctor Wicha, esto no es necesariamente un problema.
"La controversia es saludable y las preguntas acerca de las células madre cancerosas son buenas para la ciencia y, añadió, "siempre habrá controversias en esta área".
El estudio dirigido por el doctor Parada fue auspiciado en parte por los Institutos Nacionales de la Salud (R01 CA131313).
—Edward R. Winstead
Lectura adicional: "La ciencia cambiante de las células madre del cáncer".





 Le invitamos a que comparta esta publicación con sus amigos, familiares y colegas y nos ayude a continuar nuestra misión de difundir las investigaciones más recientes sobre la prevención, el tratamiento y la información del cáncer.
Le invitamos a que comparta esta publicación con sus amigos, familiares y colegas y nos ayude a continuar nuestra misión de difundir las investigaciones más recientes sobre la prevención, el tratamiento y la información del cáncer.