Información general
Mortalidad
Vigilancia de los efectos tardíos
Recursos para la atención de apoyo al superviviente
Transición a la atención del superviviente
Durante las últimas cinco décadas, se ha logrado avances notables en el establecimiento de un tratamiento para la cura de las neoplasias malignas infantiles. Se espera, que con el acceso a los tratamientos contemporáneos para las neoplasias infantiles, se espera que el 80% de los niños vivan durante mucho tiempo hasta la adultez.[1] El tratamiento responsable de esta supervivencia también puede producir, a largo plazo, resultados adversos relacionados con la salud, estos son los llamados "efectos tardíos" que se manifiestan meses o años después de finalizado el tratamiento del cáncer. Se ha utilizado una variedad de abordajes para avanzar en la comprensión de la morbilidad prolongada que se relaciona con el cáncer infantil y su contribución a una mortalidad temprana. Estas iniciativas han utilizado un espectro de recursos que incluye el análisis de los datos de registros demográficos, los resultados autonotificados proporcionados mediante estudios demográficos a gran escala con cohortes e información recopilada de las evaluaciones médicas. Los estudios sobre informes en cuanto a los resultados en supervivientes bien caracterizados en cuanto al estado clínico y su exposición a tratamientos, y que evaluaron de manera integral efectos específicos mediante análisis médicos, generalmente proporcionan la calidad más alta de datos a fin de establecer la cantidad de episodios y perfiles de riesgo de toxicidad tardía relacionada con el tratamiento del cáncer. Independientemente de la metodología de un estudio, es importante tomar en cuenta el sesgo de selección y participación de los estudios de cohorte en el contexto de los hallazgos notificados.
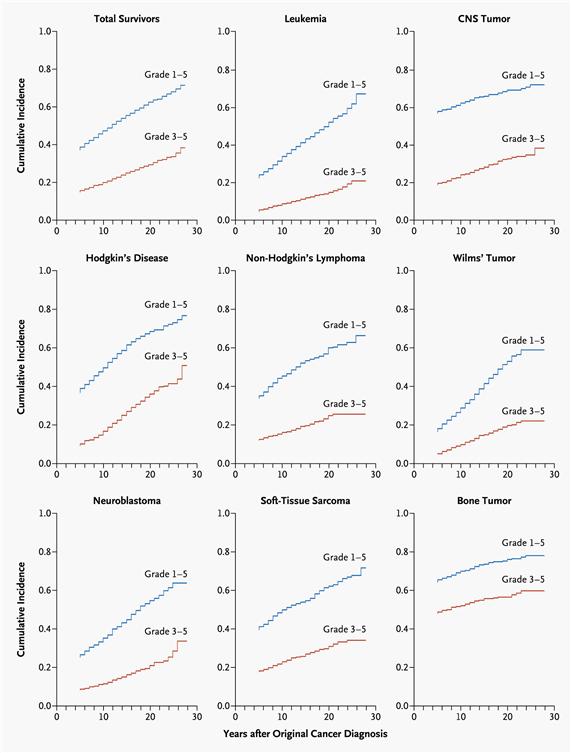
Generalmente, quienes presentan efectos tardíos son adultos que sobrevivieron al cáncer durante la niñez y muestran un aumento en la prevalencia relacionada tiempo transcurrido a partir del diagnóstico del cáncer. Los estudios demográficos sustentan el exceso de morbilidad relacionada con la morbilidad hospitalaria entre los supervivientes del cáncer infantil en comparación con los controles ajustada por edad y sexo.[3-6] La investigación mostró claramente que los efectos tardíos contribuyen a una carga alta de morbilidad entre los adultos tratados por cáncer durante la niñez: donde 60 hasta casi 90% presentan una o más afecciones crónicas y entre 20 y 40% presentan complicaciones graves o potencialmente mortales durante la edad adulta.[2,7-10] El reconocimiento de los efectos tardíos, junto con los adelantos en la biología del cáncer, las ciencias radiológicas y la atención de apoyo dio como resultado un cambio en la prevalencia y el espectro de los efectos del tratamiento. Con la finalidad de reducir y prevenir los efectos tardíos, el tratamiento contemporáneo de la mayoría de las neoplasias malignas infantiles evolucionó hacia un abordaje adaptado al riesgo que se asigna con base en una variedad de factores clínicos, biológicos, y a veces, genéticos. Con excepción de los supervivientes que necesitan un tratamiento intensivo multimodal por neoplasias malignas dinámicas resistentes al tratamiento o recidivantes, los efectos potencialmente mortales del tratamiento en el seguimiento temprano (hasta 10 años después del diagnóstico) son relativamente poco comunes después de los tratamientos contemporáneos. Sin embargo, los supervivientes todavía presentan con frecuencia una morbilidad que altera la calidad de vida debido a los efectos del tratamiento del cáncer en el funcionamiento endocrino, reproductivo, musculoesquelético y neurológico.
MortalidadLos efectos tardíos también contribuyen a un exceso de riesgo de muerte prematura entre los superviviente de cáncer infantil a largo plazo. Varios estudios de cohortes muy grandes con supervivientes notificaron mortalidad temprana entre los individuos que se trataron por cáncer infantil comparados con controles de la población general y ajustados por edad y sexo. El cáncer primario que recae o es resistente al tratamiento sigue siendo la causa más frecuente de defunción, seguido de una mortalidad excesiva por causa específica debido a cánceres primarios subsiguientes y toxicidad cardíaca y pulmonar.[11-18][Grado de comprobación: 3iA] A pesar de las tasas altas de morbilidad prematura, la mortalidad general ha disminuido con el transcurso del tiempo.[19,20] Esta reducción se relaciona con una disminución en las defunciones por cáncer primario sin estar esto vinculado con un aumento de la mortalidad por cánceres subsiguientes o toxicidades relacionadas con el tratamiento. La primera refleja mejorías en la eficacia terapéutica y el último refleja los cambios en el tratamiento posterior al estudio de las causas de los efectos tardíos. La expectativa de que las tasas de mortalidad de los supervivientes seguirán excediendo a las de la población general se basa en las secuelas a largo plazo que tienen probabilidad de aumentar con la edad alcanzada.[19] Si se realiza un seguimiento a los pacientes tratados con protocolos terapéuticos durante períodos prolongados hasta la edad adulta, será posible evaluar el exceso de mortalidad de por vida que se relaciona con intervenciones terapéuticas específicas.
Vigilancia de los efectos tardíosEl reconocimiento tanto de la toxicidad aguda o específica tardía, dio lugar a que se realizaran investigaciones que evaluaran la fisiopatología y los factores pronósticos de los efectos relacionados con el tratamiento del cáncer. Los resultados de estos estudios desempeñaron una función importante en el cambio de enfoques terapéuticos para el cáncer infantil y en la reducción de la mortalidad relacionada con el tratamiento entre supervivientes tratados en épocas más recientes.[20] Estas investigaciones también dieron cuenta del establecimiento de recomendaciones para la orientación relacionada con los riesgos y los exámenes médicos de los supervivientes a largo plazo al identificar las características clínicas y de tratamiento de quienes presentan el riesgo más alto de complicaciones relacionadas con el tratamiento. Los efectos tardíos comunes al cáncer infantil abarcan varios dominios amplios que incluyen el crecimiento y el desarrollo, el funcionamiento orgánico, la capacidad reproductiva, la salud de la descendencia del paciente y la carcinogénesis secundaria. Además, los supervivientes de cáncer infantil pueden presentar una variedad de secuelas psicosociales adversas relacionadas con el cáncer primario, su tratamiento o la falta de adaptación relacionada con la vivencia del cáncer.
Las secuelas tardías debido al tratamiento del cáncer infantil se pueden anticipar sobre la base de exposiciones terapéuticas, pero la magnitud del riesgo sus manifestaciones en un paciente en particular se ven influidas por numerosos factores. Los factores que se deben tomar en cuenta en la evaluación de riesgos de un determinado efecto tardío incluyen los siguientes:
Factores relacionados con el tumor
- Localización del tumor.
- Efectos directos en el tejido.
- Disfunción orgánica inducida por el tumor.
- Efectos mecánicos.
Factores relacionados con el tratamiento
- Radioterapia: dosis totales, tamaño de la fracción, volumen del órgano o tejido y tipo de energía de la máquina.
- Quimioterapia: tipo de sustancia, intensidad de las dosis, dosis acumulada, esquema de administración.
- Cirugía: técnica, sitio.
- Uso de terapia de modalidad combinada.
- Transfusión de hemoderivados.
- Trasplante de células hematopoyéticas.
Factores relacionados con el huésped
- Sexo.
- Edad en el momento del diagnóstico.
- Tiempo transcurrido desde el diagnóstico o el tratamiento.
- Estadio de desarrollo.
- Predisposición genética.
- Sensibilidades relacionadas con el tejido y la capacidad de reparación del tejido normal.
- Estado premórbido de salud.
- Condición socioeconómica.
- Hábitos de salud.
La American Society of Pediatric Hematology/Oncology, la International Society of Pediatric Oncology, la American Academy of Pediatrics, el Children’s Oncology Group (COG), y el Institute of Medicine apoyan la necesidad de un seguimiento a largo plazo de los supervivientes de cáncer infantil. En concreto, se recomienda un seguimiento médico con base en el riesgo, que incluya un plan sistemático para la identificación, vigilancia y prevención de por vida y que incorpore cálculos de riesgo con base en el cáncer anterior, el tratamiento del cáncer, la predisposición genética, los comportamientos relacionados con el modo de vida y las afecciones comórbidas.[21,22] Parte del seguimiento a largo plazo también se debe enfocar en la identificación sistemática apropiada del avance educativo y vocacional. Los tratamientos específicos para el cáncer infantil, especialmente aquellos que repercuten directamente en las estructuras del sistema nervioso, pueden resultar en déficits sensoriales, motrices y neurocognitivos que pueden tener consecuencias adversas en el estado funcional, los logros educativos y las oportunidades vocacionales futuras.[23] En una investigación del Childhood Cancer Survivor Study (CCSS), se observó que el tratamiento con dosis de radiación craneal de 25 Gy o más, se relacionó con mayores probabilidades de desempleo (relacionado con la salud: oportunidad relativa [OR] = 3,47; intervalo de confianza [IC] 95%, 2,54–4,74; búsqueda de trabajo: OR = 1,77; IC 95%, 1,15–2,71).[24] Los supervivientes desempleados notificaron grados más altos de funcionamiento físico precario que los supervivientes empleados, tenían educación e ingresos inferiores y era más probable que estuvieran asegurados por el sistema público que los hermanos desempleados.[24] Estos datos recalcan la importancia de facilitar el acceso de los supervivientes a los servicios correctivos, que demostraron incidir positivamente en los logros educacionales [25] que, a su vez, pueden mejorar las oportunidades vocacionales.
Además de la identificación sistemática sustentada en el riesgo de los efectos tardíos del tratamiento, también se debe enfatizar la repercusión de los comportamientos de salud sobre los riesgos para la misma relacionados con el cáncer. Los comportamientos que fomentan la salud se deben enfatizar en los supervivientes del cáncer infantil porque los esfuerzos educativos dirigidos parecen valer la pena.[26-29] El tabaquismo, el consumo excesivo de alcohol y el consumo de drogas ilícitas aumentan el riesgo de toxicidad orgánica y, posiblemente, neoplasias malignas subsiguientes. Las prácticas alimentarias nocivas para la salud y el modo de vida sedentario pueden exacerbar las complicaciones metabólicas y cardiovasculares relacionadas con el tratamiento. El abordaje dinámico de los hábitos nocivos y peligrosos es pertinente, como lo confirman varias investigaciones de supervivientes a largo plazo que consumen tabaco y alcohol, y ejercitan modos de vida inactivos que se traducen en tasas más altas que las ideales debido a su mayor riesgo de efectos tardíos cardíacos, pulmonares y metabólicos.[30-32]
Desafortunadamente, la mayoría de los supervivientes de cáncer infantil no reciben una atención sustentada en el riesgo como se recomienda. El CCSS informó que 88,8% de los supervivientes recibían alguna forma de atención médica; sin embargo, solo 31,5% notificó recibir atención enfocada en su cáncer previo (atención fundamentada en el superviviente) y 17,8 % notificó recibir atención enfocada en el superviviente que incluía asesoramiento acerca de la reducción de riesgos y discusión, u órdenes de pruebas de detección.[30] En el seno de la misma cohorte, la vigilancia de casos nuevos de cáncer fue muy baja para los supervivientes en riesgo más alto de contraer cáncer de colon, mama o piel; ello indica que los supervivientes y sus médicos necesitan educarse acerca de sus riesgos y la vigilancia recomendada.[33] El acceso al seguro de enfermedad parece desempeñar una función importante en el acceso a la atención de los supervivientes según su riesgo. En un estudio relacionado del CCSS, los supervivientes no asegurados tuvieron menores probabilidades que quienes tenían acceso a un seguro privado, desinformar una visita relacionada con el cáncer (riesgo relativo ajustado [RR] = 0,83; IC 95%, 0,75–0,91) o una visita a un centro de oncología (RR ajustado = 0,83; IC 95%, 0,71–0,98). Los supervivientes no asegurados tenían niveles inferiores de utilización en todas las medidas de atención comparadas con los supervivientes con acceso a un seguro privado. En contraste, los supervivientes con seguro público tenían mayores probabilidades de notificar una visita relacionada con el cáncer (RR ajustado = 1,22; IC 95%, 1,11–1,35) o una visita a un centro de oncología (RR ajustado = 1,41; IC 95%, 1,18–1,70) que los supervivientes con seguro privado.[34] En términos generales, la falta de seguro de enfermedad sigue siendo una preocupación importante para los supervivientes de cáncer infantil debido a cuestiones de salud, desempleo y otros factores sociales. La legislación, como la de la Health Insurance Portability y el Accountability Act mejoró el acceso al seguro de enfermedad y la retención del mismo para los supervivientes, aunque no se estudió bien la calidad y las limitaciones relacionadas con estas política.[35,36]
Transición a la atención del supervivienteLa transición de la atención pediátrica al entorno de salud para adultos es necesaria para la mayoría de los supervivientes de cáncer infantil en los Estados Unidos. Cuando se dispone de ellos, los programas multidisciplinarios de seguimiento a largo plazo (SLP) en el centro de cáncer infantil trabajan en colaboración con los médicos de la comunidad para prestar atención a los supervivientes de cáncer infantil. Este tipo de atención compartida se propuso como modelo óptimo para facilitar la coordinación entre el equipo del centro de oncología y los grupos médicos de la comunidad que proporcionan atención a los supervivientes.[37] Un servicio esencial de los programas de SLP es la organización de un plan de atención individualizado de supervivencia que incluye detalles acerca de las intervenciones terapéuticas administradas contra el cáncer infantil y sus potenciales riesgos para la salud, las recomendaciones de exámenes médicos personalizadas y la información acerca de los factores de estilos de vida que modifican los riesgos. Para los supervivientes que no recibieron esta información, el COG ofrece una plantilla que los supervivientes pueden usar para organizar un resumen del tratamiento personal (consultar el documento en inglés Survivorship Guidelines Appendix 1).
Para facilitar el acceso al superviviente y al proveedor de información sucinta que guie la atención sustentada en el riesgo, los investigadores del COG organizaron un compendio de recomendaciones de vigilancia sanitaria con base en la exposición y el riesgo con la meta de estandarizar la atención de los supervivientes de cáncer infantil.[21] Las Long-Term Follow-Up Guidelines for Survivors of Childhood, Adolescent and Young Adult Cancers del COG resultan apropiadas para supervivientes asintomáticos que se presentan para un seguimiento médico de rutina que se basa en una exposición de dos años o más después de finalizar el tratamiento. Los materiales educativos para los pacientes, que se llaman "Health Links'' (Enlaces de salud) suministran información en detalle con directrices sobre temas específicos para mejorar el mantenimiento y la promoción de la salud en esta población de supervivientes de cáncer.[38] Los grupos multidisciplinarios de trabajo que se sustentan en los sistemas (por ejemplo, cardiovascular, neurocognitivo y reproductivo), que son responsables de darle seguimiento a la literatura médica, evaluar el contenido de las directrices y proporcionar recomendaciones para la revisión de directrices a medida que se dispone de información nueva, también publicaron varios revisiones integrales que abordan los efectos tardíos específicos del cáncer infantil.[39-47] La información concerniente a los efectos tardíos se resume en los cuadros de todo este sumario.
Bibliografía
- Jemal A, Siegel R, Xu J, et al.: Cancer statistics, 2010. CA Cancer J Clin 60 (5): 277-300, 2010 Sep-Oct. [PUBMED Abstract]
- Oeffinger KC, Mertens AC, Sklar CA, et al.: Chronic health conditions in adult survivors of childhood cancer. N Engl J Med 355 (15): 1572-82, 2006. [PUBMED Abstract]
- Lorenzi MF, Xie L, Rogers PC, et al.: Hospital-related morbidity among childhood cancer survivors in British Columbia, Canada: report of the childhood, adolescent, young adult cancer survivors (CAYACS) program. Int J Cancer 128 (7): 1624-31, 2011. [PUBMED Abstract]
- Mols F, Helfenrath KA, Vingerhoets AJ, et al.: Increased health care utilization among long-term cancer survivors compared to the average Dutch population: a population-based study. Int J Cancer 121 (4): 871-7, 2007. [PUBMED Abstract]
- Sun CL, Francisco L, Kawashima T, et al.: Prevalence and predictors of chronic health conditions after hematopoietic cell transplantation: a report from the Bone Marrow Transplant Survivor Study. Blood 116 (17): 3129-39; quiz 3377, 2010. [PUBMED Abstract]
- Rebholz CE, Reulen RC, Toogood AA, et al.: Health care use of long-term survivors of childhood cancer: the British Childhood Cancer Survivor Study. J Clin Oncol 29 (31): 4181-8, 2011. [PUBMED Abstract]
- Geenen MM, Cardous-Ubbink MC, Kremer LC, et al.: Medical assessment of adverse health outcomes in long-term survivors of childhood cancer. JAMA 297 (24): 2705-15, 2007. [PUBMED Abstract]
- Wasilewski-Masker K, Mertens AC, Patterson B, et al.: Severity of health conditions identified in a pediatric cancer survivor program. Pediatr Blood Cancer 54 (7): 976-82, 2010. [PUBMED Abstract]
- Stevens MC, Mahler H, Parkes S: The health status of adult survivors of cancer in childhood. Eur J Cancer 34 (5): 694-8, 1998. [PUBMED Abstract]
- Garrè ML, Gandus S, Cesana B, et al.: Health status of long-term survivors after cancer in childhood. Results of an uniinstitutional study in Italy. Am J Pediatr Hematol Oncol 16 (2): 143-52, 1994. [PUBMED Abstract]
- Armstrong GT, Liu Q, Yasui Y, et al.: Late mortality among 5-year survivors of childhood cancer: a summary from the Childhood Cancer Survivor Study. J Clin Oncol 27 (14): 2328-38, 2009. [PUBMED Abstract]
- Bhatia S, Robison LL, Francisco L, et al.: Late mortality in survivors of autologous hematopoietic-cell transplantation: report from the Bone Marrow Transplant Survivor Study. Blood 105 (11): 4215-22, 2005. [PUBMED Abstract]
- Dama E, Pastore G, Mosso ML, et al.: Late deaths among five-year survivors of childhood cancer. A population-based study in Piedmont Region, Italy. Haematologica 91 (8): 1084-91, 2006. [PUBMED Abstract]
- Lawless SC, Verma P, Green DM, et al.: Mortality experiences among 15+ year survivors of childhood and adolescent cancers. Pediatr Blood Cancer 48 (3): 333-8, 2007. [PUBMED Abstract]
- MacArthur AC, Spinelli JJ, Rogers PC, et al.: Mortality among 5-year survivors of cancer diagnosed during childhood or adolescence in British Columbia, Canada. Pediatr Blood Cancer 48 (4): 460-7, 2007. [PUBMED Abstract]
- Möller TR, Garwicz S, Perfekt R, et al.: Late mortality among five-year survivors of cancer in childhood and adolescence. Acta Oncol 43 (8): 711-8, 2004. [PUBMED Abstract]
- Tukenova M, Guibout C, Hawkins M, et al.: Radiation therapy and late mortality from second sarcoma, carcinoma, and hematological malignancies after a solid cancer in childhood. Int J Radiat Oncol Biol Phys 80 (2): 339-46, 2011. [PUBMED Abstract]
- Reulen RC, Winter DL, Frobisher C, et al.: Long-term cause-specific mortality among survivors of childhood cancer. JAMA 304 (2): 172-9, 2010. [PUBMED Abstract]
- Armstrong GT, Pan Z, Ness KK, et al.: Temporal trends in cause-specific late mortality among 5-year survivors of childhood cancer. J Clin Oncol 28 (7): 1224-31, 2010. [PUBMED Abstract]
- Yeh JM, Nekhlyudov L, Goldie SJ, et al.: A model-based estimate of cumulative excess mortality in survivors of childhood cancer. Ann Intern Med 152 (7): 409-17, W131-8, 2010. [PUBMED Abstract]
- Landier W, Bhatia S, Eshelman DA, et al.: Development of risk-based guidelines for pediatric cancer survivors: the Children's Oncology Group Long-Term Follow-Up Guidelines from the Children's Oncology Group Late Effects Committee and Nursing Discipline. J Clin Oncol 22 (24): 4979-90, 2004. [PUBMED Abstract]
- Oeffinger KC, Hudson MM: Long-term complications following childhood and adolescent cancer: foundations for providing risk-based health care for survivors. CA Cancer J Clin 54 (4): 208-36, 2004 Jul-Aug. [PUBMED Abstract]
- Hudson MM, Mulrooney DA, Bowers DC, et al.: High-risk populations identified in Childhood Cancer Survivor Study investigations: implications for risk-based surveillance. J Clin Oncol 27 (14): 2405-14, 2009. [PUBMED Abstract]
- Kirchhoff AC, Leisenring W, Krull KR, et al.: Unemployment among adult survivors of childhood cancer: a report from the childhood cancer survivor study. Med Care 48 (11): 1015-25, 2010. [PUBMED Abstract]
- Mitby PA, Robison LL, Whitton JA, et al.: Utilization of special education services and educational attainment among long-term survivors of childhood cancer: a report from the Childhood Cancer Survivor Study. Cancer 97 (4): 1115-26, 2003. [PUBMED Abstract]
- Cox CL, McLaughlin RA, Rai SN, et al.: Adolescent survivors: a secondary analysis of a clinical trial targeting behavior change. Pediatr Blood Cancer 45 (2): 144-54, 2005. [PUBMED Abstract]
- Cox CL, McLaughlin RA, Steen BD, et al.: Predicting and modifying substance use in childhood cancer survivors: application of a conceptual model. Oncol Nurs Forum 33 (1): 51-60, 2006. [PUBMED Abstract]
- Cox CL, Montgomery M, Oeffinger KC, et al.: Promoting physical activity in childhood cancer survivors: results from the Childhood Cancer Survivor Study. Cancer 115 (3): 642-54, 2009. [PUBMED Abstract]
- Cox CL, Montgomery M, Rai SN, et al.: Supporting breast self-examination in female childhood cancer survivors: a secondary analysis of a behavioral intervention. Oncol Nurs Forum 35 (3): 423-30, 2008. [PUBMED Abstract]
- Nathan PC, Ford JS, Henderson TO, et al.: Health behaviors, medical care, and interventions to promote healthy living in the Childhood Cancer Survivor Study cohort. J Clin Oncol 27 (14): 2363-73, 2009. [PUBMED Abstract]
- Schultz KA, Chen L, Chen Z, et al.: Health and risk behaviors in survivors of childhood acute myeloid leukemia: a report from the Children's Oncology Group. Pediatr Blood Cancer 55 (1): 157-64, 2010. [PUBMED Abstract]
- Tercyak KP, Donze JR, Prahlad S, et al.: Multiple behavioral risk factors among adolescent survivors of childhood cancer in the Survivor Health and Resilience Education (SHARE) program. Pediatr Blood Cancer 47 (6): 825-30, 2006. [PUBMED Abstract]
- Nathan PC, Ness KK, Mahoney MC, et al.: Screening and surveillance for second malignant neoplasms in adult survivors of childhood cancer: a report from the childhood cancer survivor study. Ann Intern Med 153 (7): 442-51, 2010. [PUBMED Abstract]
- Casillas J, Castellino SM, Hudson MM, et al.: Impact of insurance type on survivor-focused and general preventive health care utilization in adult survivors of childhood cancer: the Childhood Cancer Survivor Study (CCSS). Cancer 117 (9): 1966-75, 2011. [PUBMED Abstract]
- Crom DB, Lensing SY, Rai SN, et al.: Marriage, employment, and health insurance in adult survivors of childhood cancer. J Cancer Surviv 1 (3): 237-45, 2007. [PUBMED Abstract]
- Pui CH, Cheng C, Leung W, et al.: Extended follow-up of long-term survivors of childhood acute lymphoblastic leukemia. N Engl J Med 349 (7): 640-9, 2003. [PUBMED Abstract]
- Oeffinger KC, McCabe MS: Models for delivering survivorship care. J Clin Oncol 24 (32): 5117-24, 2006. [PUBMED Abstract]
- Eshelman D, Landier W, Sweeney T, et al.: Facilitating care for childhood cancer survivors: integrating children's oncology group long-term follow-up guidelines and health links in clinical practice. J Pediatr Oncol Nurs 21 (5): 271-80, 2004 Sep-Oct. [PUBMED Abstract]
- Castellino S, Muir A, Shah A, et al.: Hepato-biliary late effects in survivors of childhood and adolescent cancer: a report from the Children's Oncology Group. Pediatr Blood Cancer 54 (5): 663-9, 2010. [PUBMED Abstract]
- Henderson TO, Amsterdam A, Bhatia S, et al.: Systematic review: surveillance for breast cancer in women treated with chest radiation for childhood, adolescent, or young adult cancer. Ann Intern Med 152 (7): 444-55; W144-54, 2010. [PUBMED Abstract]
- Jones DP, Spunt SL, Green D, et al.: Renal late effects in patients treated for cancer in childhood: a report from the Children's Oncology Group. Pediatr Blood Cancer 51 (6): 724-31, 2008. [PUBMED Abstract]
- Liles A, Blatt J, Morris D, et al.: Monitoring pulmonary complications in long-term childhood cancer survivors: guidelines for the primary care physician. Cleve Clin J Med 75 (7): 531-9, 2008. [PUBMED Abstract]
- Nandagopal R, Laverdière C, Mulrooney D, et al.: Endocrine late effects of childhood cancer therapy: a report from the Children's Oncology Group. Horm Res 69 (2): 65-74, 2008. [PUBMED Abstract]
- Nathan PC, Patel SK, Dilley K, et al.: Guidelines for identification of, advocacy for, and intervention in neurocognitive problems in survivors of childhood cancer: a report from the Children's Oncology Group. Arch Pediatr Adolesc Med 161 (8): 798-806, 2007. [PUBMED Abstract]
- Ritchey M, Ferrer F, Shearer P, et al.: Late effects on the urinary bladder in patients treated for cancer in childhood: a report from the Children's Oncology Group. Pediatr Blood Cancer 52 (4): 439-46, 2009. [PUBMED Abstract]
- Shankar SM, Marina N, Hudson MM, et al.: Monitoring for cardiovascular disease in survivors of childhood cancer: report from the Cardiovascular Disease Task Force of the Children's Oncology Group. Pediatrics 121 (2): e387-96, 2008. [PUBMED Abstract]
- Wasilewski-Masker K, Kaste SC, Hudson MM, et al.: Bone mineral density deficits in survivors of childhood cancer: long-term follow-up guidelines and review of the literature. Pediatrics 121 (3): e705-13, 2008. [PUBMED Abstract]


 Volver arriba
Volver arriba